Daftar isi
Dalam lingkup pembelajaran fisika ada konsep tertentu untuk mengamati pergerakan elektron dalam suatu medium tertentu. Seperti yang diketahui elektron merupakan suatu partikel sub atom yang bermuatan negatif. Atom sendiri tidak hanya tersusun atas elektron, namun ada juga proton (partikel sub atom yang bermuatan positif) dan neutron (partikel sub atom yang bermuatan netral).
Namun pada kesempatan kali ini akan difokuskan pada pembahasan elektron dan pergerakaannya. Konsep pergerakan elektron ini dikenal dengan efek fotolistrik.
Apa itu Efek Fotolistrik?
Efek fotolistrik pertama kali ditemukan oleh Heinrich Hertz pada tahun 1887. Hertz sendiri menemukan konsep efek fotolistrik ini ketika melakukan suatu eksperimen untuk mengamati fenomena radiasi. Pada eksperimen ini ada suatu fenomena terlepasnya elektron dari suatu permukaan logam ketika cahaya menumbuk logam tersebut.
Fenomena ini kemudian dikenal dengan efek fotolistrik. Elektron yang terlepas dari permukaan logam ini disebut dengan fotoelektron.
Rumus Efek Fotolistrik
Fenomena efek fotolistrik memunculkan rumusan-rumusan mengenai energi kinetik, frekuensi ambang, energi kinetik pada teori kuantum, dan panjang gelombang. Berikut adalah rumus-rumus terkait efek fotolistrik.
Rumus Energi Kinetik pada Efek Fotolistrik
Eksperimen efek fotolistrik memunculkan kesimpulan bahwa energi kinetik yang terjadi pada efek fotolistrik bergantung pada muatan elektron dan potensial henti. Rumus untuk energi kinetik pada efek fotolistrik adalah sebagai berikut.
Ekmaks = e.V0
dengan e adalah muatan elektron (C) dan V0 adalah potensial henti (volt). Potensial henti terjadi saat nilai arus sama dengan nol.
Rumus Frekuensi Ambang
Frekuensi ambang diartikan sebagai nilai frekuensi foton terendah yang mampu menimbulkan efek fotolistrik. Foton sendiri diartikan sebagai sebuah partikel elementer dalam suatu fenomena elektromagnetik.
Elektron dan foton adalah partikel yang berbeda. Foton merupakan pembawa radiasi elektromagnetik. Rumus frekuensi ambang dirumuskan sebagai berikut.
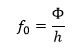
dengan h adalah konstanta planck (Js) dan Ф adalah fungsi kerja (eV).
Rumus Energi Kinetik pada Teori Kuantum
Efek fotolistrik pada model Einstein menjelaskan bahwa pada intensitas cahaya tertentu foton akan memberikan semua energi ke elektron yang ada pada plat logam.
Elektron yang keluar dari suatu permukaan plat logam tidak akan bertabrakan dengan atom yang lain sebelum energi kinetik maksimum dari elektron tersebut keluar. Berikut adalah energi kinetik maksimum bagi elektron yang terbebas.
Ekmaks = hf – Ф
dengan h adalah konstanta Planck (Js), f adalah frekuensi foton (Hz), dan Ф adalah fungsi kerja (eV). Fungsi kerja adalah energi minimum yang dibutuhkan oleh elektron agar bisa menempel pada logam.
Pada efek fotolistrik, energi kinetik tidak bergantung pada intensitas cahaya. Ketika intensitas cahaya diperbesar maka energi kinetik pada setiap elektron tidak akan berubah. Perubahan intensitas cahaya hanya akan berpengaruh terhadap jumlah elektron yang terlepas dari permukaan logam.
Energi kinetik maksimum justru dipengaruhi oleh frekuensi cahaya. Dengan mensubstitusikan rumus frekuensi ambang pada rumus Ekmaks maka diperoleh rumus sebagai berikut.
Ekmaks = h(f – f0)
Rumus Panjang Gelombang
Berdasarkan frekuensi ambang dapat pula diketahui panjang gelombang ambang dengan rumus berikut.
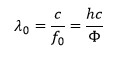
dengan λ0 adalah panjang gelombang (m), c adalah kecepatan cahaya dengan nilai 3 × 108 m/s, dan hc sama dengan 1240 eV nm.
Contoh Soal Efek Fotolistrik
Berikut adalah beberapa contoh soal mengenai efek fotolistrik disertai dengan pembahasannya.
Soal 1 dan Pembahasan
Tentukan energi kinetik elektron yang keluar dari suatu logam yang memiliki frekuensi kerja sebesar 5 × 1014 Hz dan diberi cahaya yang berfrekuensi 8 × 1014 Hz!
Pembahasan:
Dari soal diketahui informasi sebagai berikut.
f = 8 × 1014 Hz
f0 = 5 × 1014 Hz
Perlu diketahui bahwa konstanta Planck yang berlaku adalah 6,6 × 10-34 Js. Sehingga energi kinetik elektron adalah
Ek = h(f – f0)
Ek = (6,6 × 10-34)(8 × 1014 – 5 × 1014)
Ek = (6,6 × 10-34)(8 – 5) × 1014
Ek = (6,6 × 3) × 10-20
Ek = 19,8 × 10-20
Jadi energi kinetik elektron yang keluar dari logam tersebut adalah 19,8 × 10-20 J.
Soal 2 dan Pembahasan
Jika suatu logam mempunyai fungsi kerja sebesar 3,7 eV, dengan e = 1,6 × 10-19 C dan h = 6,6 × 10-34 Js, maka tentukan besar frekuensi ambang dari logam tersebut!
Pembahasan:
Dari soal diketahui informasi sebagai berikut.
Ф = 3,7 eV
e = 1,6 × 10-19 C
h = 6,6 × 10-34 Js
Frekuensi ambang dari logam adalah
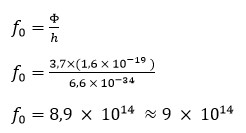
Jadi nilai frekuensi ambang dari logam tersebut pada kisaran 9 × 1014 Hz.
Soal 3 dan Pembahasan
Permukaan logam natrium disinari oleh cahaya dengan panjang gelombang 300 nm. Fungsi kerja natrium diketahui sebesar 2,46 eV. Tentukan energi kinetik maksimum yang dikeluarkan oleh fotoelektron dan panjang gelombang untuk natrium!
Pembahasan:
Berdasarkan soal diperoleh informasi sebagai berikut.
λ = 300 nm
Ф = 2,46 eV
Ingat kembali bahwa hc = 1240 eV nm
- Akan ditentukan energi kinetik maksimum yang dikeluarkan oleh fotoelektron:
Diketahui dari rumus bahwa f = c/ λ dan Ekmaks = hf – Ф, maka diperoleh

Jadi, besarnya energi kinetik maksimum yang dikeluarkan oleh fotoelektron adalah 1,67 eV
- Akan ditentukan panjang gelombang natrium:
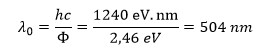
Jadi, panjang gelombang natrium adalah 504 nm.
