Daftar isi
Tahukah kamu, ketika manusia bernapas pasti akan menarik dan mengeluarkan napas sehingga volume paru-paru menjadi mengembang, lalu tekanannya menurun. Nah, sesuatu yang bisa ditarik dan dihembuskan itu adalah udara berbentuk gas.
Meskipun, gas tersebut tidak bisa dilihat. Namun, bisa dihitung melalui rumus kimia yang bernama Hukum Boyle. Selain dari sistem pernapasan makhluk hidup, Hukum Boyle juga berguna untuk alat-alat di sekitar kita.
Maka dari itu, penting bagi kita untuk memahami Hukum Boyle secara mendalam, seperti yang akan dijelaskan di bawah ini!
Apa itu Hukum Boyle?
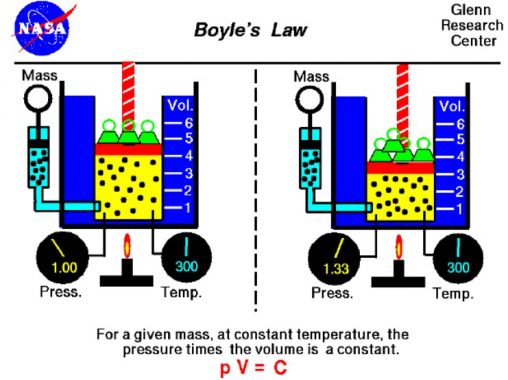
Hukum Boyle atau Hukum Mariotte adalah hukum yang berhubungan dengan sifat fisik gas, yaitu volume dan tekanan di ruang tertutup. Hukum Boyle sangat berfungsi dalam kehidupan sehari-hari, contohnya seperti penggunaan hairspray, cat pilox, dan obat nyamuk kaleng.
Bagaimana Sejarah Hukum Boyle?
Hukum Boyle ditemukan oleh ahli kimia, filsuf, fisikawan dan penulis asal Irlandia yang bernama Robert Boyle pada tahun 1662.
Pada tahun tersebut, Boyle dan Robert Hooken memperkenalkan hasil penemuan mereka kepada publik mengenai hubungan keterbalikan antara tekanan dengan volume gas, yang nantinya kita kenal sebagai “Hukum Boyle”.
Namun, Hukum Boyle juga kerap kali disebut sebagai Hukum Mariotte. Sebab, Mariotte seorang Fisikawan asal perancis, juga menemukan hukum Boyle dengan independent pada tahun1679.
Faktor Apa yang Memengaruhi Hukum Boyle?
Karena Hukum Boyle mengatakan bahwa tekanan berbanding terbalik dengan volume gas apabila suhu dalam keadaan konstan dan di ruang tertutup, maka faktor yang memengaruhi Hukum Boyle yaitu tekanan, volume dan suhu.
Apa Rumus Hukum Boyle?
Rumus Hukum Boyle menemukan bahwa hasil perkalian dari tekanan (P) dengan volume (V) hasilnya adalah bernilai konstan serta disebut sebagai konstanta gas ideal, selama suhu gas dan massa dijaga dengan konsisten.
Maka rumus tersebut ditulis secara matematis adalah sebagai berikut:
P x V = K
Keterangan:
P: tekanan gas (N/m2)
V: volume gas (m3)
K: Konstanta gas ideal
Apa Persamaan Hukum Boyle?
Agar tekanan dan volume serta gas menjadi seimbang khususnya pada suhu tetap, maka persamaannya sebagai berikut:
P1 x V1 = P2 x V2
Keterangan:
P1: tekanan awal gas di dalam ruang (N/m2 atau Pa atau atm)
V1: volume awal gas di dalam ruang (m3)
P2: tekanan akhir gas di dalam ruang (N/m2 atau Pa atau atm)
V2: volume awal gas di dalam ruang (m3)
Bagaimana Contoh Soal Hukum Boyle Beserta Pembahasannya?
Contoh soal 1
Diketahui tekanan gas berisikan 4 atm di dalam wadah tertutup, sedangkan volume gasnya adalah 1 liter. Beberapa jam kemudian, tekanan gas berubah menjadi 6 atm. Hitunglah berapa volume gas tersebut saat ini?
Pembahasan:
- P1 = 4 atm
P1 = 4 x 105 Pa
- P2 = 6 atm
P2 = 6 x 105 Pa
- V1 = 1 liter
V1 = 1 x 10-3 m3
- (4 x 105) (1 x 10-3) = (6 x 105) V2
4 x 102 = (6 x 105) V2
2/3 x 10-3 = V2
2/3 x 10-3 dm3 = V2
0,67 liter = V2
Jadi, volume gas saat ini adalah 0,67 liter.
Contoh soal 2
Diketahui jumlah awal suatu gas ideal mempunyai tekanan sejumlah P dan volume sejumlah V. Beberapa saat kemudian, tekanan gas tersebut berubah menjadi 2 kali tekanan awal. Hitunglah volume gas saat ini!
Pembahasan:
P1 x V1 = P2 x V2
P x V = 2P x V2
V = 2 x V2
½ V = V2
Jadi, volume gas saat ini adalah menjadi ½ volume gas awal.
Bagaimana Contoh Penerapan Hukum Boyle Dalam Kehidupan Manusia?
1. Pernapasan makhluk hidup
Sempat disinggung di atas bahwa sistem pernapasan makhluk hidup adalah salah satu contoh penggunaan Hukum Boyle di dalam kehidupan manusia.
Dalam proses respirasi atau saat kita bernapas, volume paru-paru akan mengembang dan tekanan akan menurun.
Sama halnya juga ketika paru-paru mengeluarkan udara, maka paru-paru akan mengempis sehingga volume berkurang dan tekanan akan meningkat. Proses tekanan dan volume tersebut disebut dengan Hukum Boyle.
2. Minuman botol soda
Keberadaan minuman botol soda menjadi salah satu wujud nyata dari penerapan Hukum Boyle. Sebab ketika botol soda tersebut dibuka maka akan terdengar suara sehingga beberapa molekul udara akan keluar.
Lalu, akan memberikan ruang bagi pergerakan molekul udara. Dan terjadilah perubahan tekanan sesuai dengan perubahan pada volume.
Tak hanya itu, ketika kita mengguncang botol tersebut dalam keadaan ditutup, maka sodanya akan mengembang dan jika dibuka akan tumpah ke luar.
Hal tersebut bisa terjadi karena gas yang ada di dalam botol tengah mencoba ke luar dan tercampur ke dalam fluida, sehingga ketika gas tersebut dilepas akan mengeluarkan cairan berbusa.
Tekanan di dalam botol tersebut menjadi turun, sedangkan volume gas menjadi naik.
3. Jarum suntik
Penerapan Hukum Boyle dalam kehidupan manusia yang terakhir adalah penggunaan jarum suntik. Pada jarum suntik terdiri dari pendorong untuk memvariasikan tekanan dan silinder untuk menampung fluida.
Ketika plunger ditekan, maka volume fluida akan berkurang dan tekanan akan meningkat. Sebaliknya, ketika plunger ditarik, maka volume akan meningkat dan tekanan akan berkurang.
